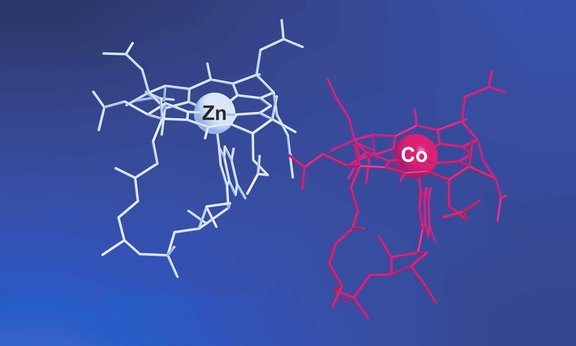
Gemeinsam mit der Forschungsgruppe um Martin J. Warren an der University of Kent ist das Team um Bernhard Kräutler in der Lage, den Grundkörper des Vitamins B12 ohne das sonst im Zentrum liegende Kobalt-Ion zu erzeugen. Diese mit genetisch modifizierten Mikroorganismen produzierten Moleküle bilden damit eine ideale Basis für die Synthese von analogen Verbindungen, in welchen andere Metalle anstelle des aktivierten Kobalt-Ions von Vitamin B12 sitzen. In einer aktuellen Arbeit in der Fachzeitschrift Angewandte Chemie International Edition präsentieren die Forscher um Christoph Kieninger und Bernhard Kräutler nun ein B12-Derivat mit einem Zink-Ion im Zentrum. „Dieses Spielen mit den Elementen ist ein alter Traum der Vitamin B12 Forschung“, freut sich Kräutler. „Damit werden sich interessante Erkenntnisse über die biologischen Funktionen von Vitamin B12 ergeben.“
Biologisch tot
Obwohl die 2-wertigen Kobalt- und Zink-Ionen praktisch gleich groß sind, verhält sich Zink im Zentrum des Corrin-Rings von Vitamin B12 anders als Kobalt. Denn während Kobalt-Ionen über eine nur teilweise mit Elektronen befüllte Valenzschale verfügen, ist diese im Zink-Ion bis auf den letzten Platz voll. „Man könnte sagen, Zink hat eine harte Schale und passt (anders als die Kobalt-Ionen) trotz gleicher Größe nicht gut in den Corrin-Ring hinein, wie die Röntgenstrukturanalyse zeigt“ erklärt Bernhard Kräutler. Aufgrund seiner elektronischen Eigenschaften kann der Zinkkomplex auch nicht die biologisch relevante, organometallische Katalyse-Aktivität des Vitamins entfalten. „Er ist biologisch tot“, resümiert Kräutler.
Als Antivitamin einsetzbar
Dies bedeutet jedoch nicht, dass die Verbindung für die biologische und biomedizinische Forschung uninteressant wäre. So kann der Zinkkomplex als perfekter Inhibitor von B12 Anwendung finden. Antivitamine B12 sind sehr wirksame Antibiotika und eines davon hat sich bei multiresistenten Keimen bereits als sehr hilfreiches Mittel erwiesen. Auch in der Krebstherapie gibt es Ansätze für den Einsatz von Antivitaminen B12, denn Tumorzellen sind hungrig nach dem Vitamin B12. Allerdings hatten die bisherigen Untersuchungen hier noch keine Erfolge. Weitere Anwendungen können sich aus den lumineszierenden Eigenschaften der Zinkverbindung ergeben. So werden in der photodynamischen Therapie mittels Lichteinstrahlung reaktive Sauerstoffspezies in Tumoren erzeugt und damit die Krebszellen bekämpft. Der fluoreszierende Zinkkomplex könnte in einfachen Tiermodellen auch dazu verwendet werden, die Mobilität von B12 und die Orte seiner Akkumulation in deren Körper zu studieren. Als einschränkend für die möglichen Anwendungen der Zinkvarianten von B12 erweist sich freilich, dass sie nicht sehr robust sind und ihre Herstellung immer noch sehr aufwändig ist.
Links
- Zinc Substitution of Cobalt in Vitamin B12: Zincobyric acid and Zincobalamin as Luminescent Structural B12‐Mimics. Christoph Kieninger, Joseph A. Baker, Maren Podewitz, Klaus Wurst, Steffen Jockusch, Andrew D. Lawrence, Evelyne Deery, Karl Gruber, Klaus R. Liedl, Martin J. Warren, Bernhard Kräutler. Angewandte Chemie International Edition 58 (41), 14568-14572
- Arbeitsgruppe Kräutler
- Institut für Organische Chemie
- Center for Molecular Biosciences Innsbruck (CMBI)