Ass.-Prof. Dr. Gergely Kali
Polymere für biomedizinische Anwendungen

Gegenstand der Arbeitsgruppe ist die interdisziplinäre Forschung an der Schnittstelle von Polymerchemie, Polysacchariden, Supramolekülen und Wirkstofftransport. Unsere Arbeit umfasst die Synthese von Polymeren und Supramolekülen unter Verwendung moderner kontrollierter Polymerisationstechniken, die Funktionalisierung verschiedener Makromoleküle mit biorelevanten Gruppen sowie Studien zum Wirkstofftransport.
Wir untersuchen zwei Hauptwege der Arzneimittelaufnahme. Der erste ist der mukosale Weg unter Verwendung mukoadhäsiver Materialien wie thiolierten, ungesättigten und kationischen Oligomeren und Polymeren. Dieser Weg ist besonders relevant, da eine Reihe wichtiger pharmazeutischer Wirkstoffe lediglich eine kurz Verweildauer auf den mit Schleimhaut bedeckten Absorptionsmembranen (beispielsweise im Magen-Darm-Trakt) aufweisen. Dies führt zu einer geringen systemischen Absorption oder reduzierten lokalen Effekten. Darüber hinaus arbeiten wir an der Optimierung der zellulären Aufnahme mit ähnlich funktionalisierten Makromolekülen.
Diese neuartigen Polymere zeichnen sich durch ihre Sicherheit, Eignung für die Arzneimittelverabreichung und den verbesserten Komfort für den Patienten aus.
Cyclodextrine sind zyklische Oligosaccharide, die in der Biomedizin bereits weit verbreitet zum Einsatz kommen. Wir modifizieren diese Makrozyklen um ihre mukoadhäsiven Eigenschaften zu optimieren, die Membranpermeabilität zu erhöhen oder die zelluläre Aufnahme zu steigern. Thiolierte Cyclodextrine werden hauptsächlich über zwei Reaktionswege synthetisiert. Ein hoher Thiolierungsgrad kann durch Reaktion mit Phosphorpentasulfid erreicht werden. Mit dieser Methode kann eine vollständige Thiolierung erzielt werden. S-Acetylmercaptobernsteinsäureanhydrid bildet Esterbindungen mit Hydroxylgruppen und sorgt so sowohl für Thiolierung als auch für eine hohe Wasserlöslichkeit. Darüber hinaus sind wir daran interessiert, weitere Funktionalisierungen von Cyclodextrinen zu untersuchen, wie beispielsweise die Derivatisierung mit kationischen oder ungesättigten Gruppen. In diesen Reaktionen finden auch eine Vielzahl weiterer Polysaccharide Anwendung, darunter Stärke, Cellulose, Chitosan und Carrageen.
Die Synthese von Polymeren erfolgt hauptsächlich unter Verwendung reversibler Deaktivierungs-Radikalpolymerisationstechniken wie der Atomtransfer-Radikalpolymerisation (ATRP) oder der reversiblen Additions-Fragmentierungs-Kettenübertragung (RAFT). Sulfhydrylgruppen oder ungesättigte Funktionalitäten werden eingesetzt, um mukoadhäsive Eigenschaften hinzuzufügen oder die zelluläre Aufnahme dieser Hilfsstoffe zu verbessern.
Der Fokus unserer Forschung liegt auf innovativen Drug Delivery Systemen aus synthetischen Polymeren. Die Polymerisation von Myrcen, einem Monoterpenoid, erzeugt ein Material mit kontrollierter Mikrostruktur und mukoadhäsiven Eigenschaften. Außerdem sind diese Polymere antioxidative und antimikrobiell. Aus diesem Grund werden sie als aktive pharmazeutische Hilfsstoffe bezeichnet. Die Polykondensation von Polyether-Glykolen (PEG) mit 2-Sulfanylbernsteinsäure oder Maleinsäureanhydrid in Kombination mit Modellwirkstoffen führt zu einem mukoadhäsiven Polymer, das in seiner Struktur polymerisierte pharmazeutische Wirkstoffe enthält. Dieses Material ermöglicht eine nachhaltige Wirkstofffreisetzung an der Anwendungsstelle.
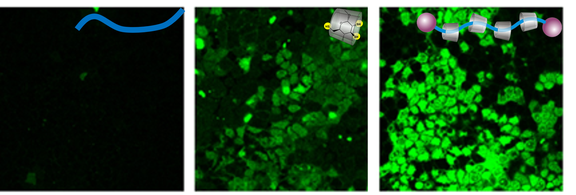
Polyrotaxane sind supramolekulare Strukturen, die aus polymeren Achsen und aufgefädelten Makrozyklen bestehen. Wir synthetisieren diese Materialien, um die zelluläre Aufnahme der Makrozyklen zu verbessern und ihre membranschädigenden Effekte zu reduzieren.
Wir untersuchen die Synthesemöglichkeiten von Polyrotaxanen unter Verwendung von Fädel- und Rotaxa-Polymerisationsmethoden. Unser Hauptziel ist es, zu verstehen, wie funktionelle Gruppen die zelluläre Aufnahme von Polyrotaxanen beeinflussen, und potenzielle Abbauwege im Zytosol zu identifizieren, die zur Freisetzung von Makrozyklen führen.
