Kein Leben ohne Metalle
Prof. Bernhard Kräutler vom Institut für Organische Chemie und Prof. Reinhard Dallinger vom Institut für Zoologie, beide Mitglieder des Centrums für Molekulare Biowissenschaften der Universität Innsbruck (CMBI), wurden von den Organisatoren der Tagung zu Vorträgen über ihre aktuellen Forschungsarbeiten eingeladen. An der kurz „CanBic-Meeting“ genannten Konferenz nehmen seit Dienstag Wissenschaftler aus aller Welt teil. Im Zentrum der bis Samstag laufenden Tagung stehen biologisch-chemische Fragen rund um Wechselwirkungen von Metallen in Lebensprozessen.
Bausatz aus der Natur
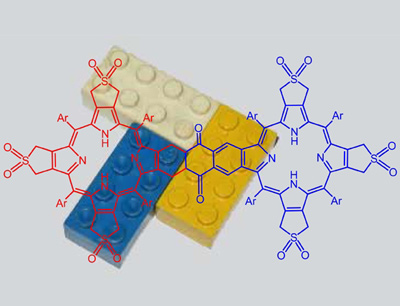
 Prof. Kräutler eröffnet in der Session „Advances in Porphyrin Chemistry“ Einblicke in seine Forschungen zu Porphyrinen. Das sind natürlich vorkommende Farbstoffe. Sie sind für viele lebenswichtige Prozesse eine chemische Grundlage. Zum Beispiel ist der Sauerstofftransporter Häm für die Farbe der roten Blutkörperchen verantwortlich oder das grüne Pflanzenpigment Chlorophyll ist die chemische Basis für die Photosynthese in Pflanzen. In seinem Vortrag mit dem Titel “Porphyrin-Assemblies Generated with Porphyrin-LEGO®“, erklärt der Wissenschaftler, wie aus relativ einfachen, von der Natur abgeschauten molekularen Bausteinen (ähnlich dem Chlorophyll und dem Häm), nach dem LEGO-Bauprinzip, Porphyrin-Komplexe hergestellt werden können. Die Gruppe rund um den Innsbrucker Chemiker hat ein Verfahren entwickelt, mit dem – ähnlich einem molekularen LEGO-Bausatz – aus Porphyrinen systematisch komplexere Porphyrin-Supermoleküle zusammengesetzt werden können. Laut Kräutler sind diese Supermoleküle als Licht absorbierende molekulare Module von besonderem Interesse. Sie könnten in der Solarenergie eingesetzt werden (Abbildung 1 links). Kräutler hält im Anschluss an die Tagung in Parry Sound auch noch einen Plenarvortrag bei der Jahrestagung der Kanadischen Chemischen Gesellschaft (CSC) in Quebec City. Dort berichtet er über aktuellste Forschungsarbeiten seiner Gruppe zum medizinisch und biologisch wichtigen Vitamin B12. Dem Team des Chemikers gelang es vor Kurzem, ein funktionsfähiges Antivitamin B12 herzustellen. Dies ist für die Erforschung des Einflusses von B12 auf Erkrankungen des Nervensystems bedeutend. (Abbildung 1 rechts).
Prof. Kräutler eröffnet in der Session „Advances in Porphyrin Chemistry“ Einblicke in seine Forschungen zu Porphyrinen. Das sind natürlich vorkommende Farbstoffe. Sie sind für viele lebenswichtige Prozesse eine chemische Grundlage. Zum Beispiel ist der Sauerstofftransporter Häm für die Farbe der roten Blutkörperchen verantwortlich oder das grüne Pflanzenpigment Chlorophyll ist die chemische Basis für die Photosynthese in Pflanzen. In seinem Vortrag mit dem Titel “Porphyrin-Assemblies Generated with Porphyrin-LEGO®“, erklärt der Wissenschaftler, wie aus relativ einfachen, von der Natur abgeschauten molekularen Bausteinen (ähnlich dem Chlorophyll und dem Häm), nach dem LEGO-Bauprinzip, Porphyrin-Komplexe hergestellt werden können. Die Gruppe rund um den Innsbrucker Chemiker hat ein Verfahren entwickelt, mit dem – ähnlich einem molekularen LEGO-Bausatz – aus Porphyrinen systematisch komplexere Porphyrin-Supermoleküle zusammengesetzt werden können. Laut Kräutler sind diese Supermoleküle als Licht absorbierende molekulare Module von besonderem Interesse. Sie könnten in der Solarenergie eingesetzt werden (Abbildung 1 links). Kräutler hält im Anschluss an die Tagung in Parry Sound auch noch einen Plenarvortrag bei der Jahrestagung der Kanadischen Chemischen Gesellschaft (CSC) in Quebec City. Dort berichtet er über aktuellste Forschungsarbeiten seiner Gruppe zum medizinisch und biologisch wichtigen Vitamin B12. Dem Team des Chemikers gelang es vor Kurzem, ein funktionsfähiges Antivitamin B12 herzustellen. Dies ist für die Erforschung des Einflusses von B12 auf Erkrankungen des Nervensystems bedeutend. (Abbildung 1 rechts).
Zukunftsweisende Modell-Moleküle aus dem Schneckenreich
 Geht es nach den jüngsten Ergebnissen, die Prof. Dallinger beim CanBic Meeting präsentiert, so könnte unsere heimische Weinbergschnecke (Helix pomatia) ein Schlüssel zum allgemein verbesserten Verständnis von Eiweißstoffen und deren Rolle bei der Bindung und Entgiftung von Metallen sein. Metallothioneine sind unter anderem bei Tieren für zahlreiche Prozesse überlebenswichtig. Schnecken (Gastropoden) können durch diese Eiweißstoffe unter anderem das toxische Schwermetall Cadmium in hohen Konzentrationen binden und entgiften. Proteine der Klasse der Metallothioneine enthalten besonders viele Aminosäuren mit Schwefelatomen (so genannte „Cysteine“). Diese können Metalle binden.
Geht es nach den jüngsten Ergebnissen, die Prof. Dallinger beim CanBic Meeting präsentiert, so könnte unsere heimische Weinbergschnecke (Helix pomatia) ein Schlüssel zum allgemein verbesserten Verständnis von Eiweißstoffen und deren Rolle bei der Bindung und Entgiftung von Metallen sein. Metallothioneine sind unter anderem bei Tieren für zahlreiche Prozesse überlebenswichtig. Schnecken (Gastropoden) können durch diese Eiweißstoffe unter anderem das toxische Schwermetall Cadmium in hohen Konzentrationen binden und entgiften. Proteine der Klasse der Metallothioneine enthalten besonders viele Aminosäuren mit Schwefelatomen (so genannte „Cysteine“). Diese können Metalle binden.
Wie Dallingers Gruppe auf Basis langjähriger Detektivarbeit im Labor herausfand, sind durch Mutationen dieser Aminosäuren im Verlauf der Gastropoden-Evolution zwei Metallothioneine mit Bindungspräferenzen für unterschiedliche Metalle entstanden (Abbildung 2). Das ermöglicht den Schnecken einerseits Cadmium in weitaus höheren Konzentrationen anzureichern und zu tolerieren, als die meisten anderen Tierarten. Auf der anderen Seite können diese wehrhaften Weichtiere das für ihren Stoffwechsel überlebenswichtige Kupfer in ihren Zellen festhalten und speichern. Weinbergschnecken benötigen Kupfer für ihre Atmung. Die Bedeutung dieser Erkenntnis liegt unter anderem darin, dass sich Schnecken-Metallothioneine deshalb als Modell-Moleküle für die Untersuchung metallspezifischer Eigenschaften von Proteinen eignen. Dallinger und sein Team sind einigen dieser Mechanismen dicht auf der Spur und leisten im zukunftsweisenden Forschungsfeld der molekularen Physiologie seit langen Jahren international renommierte Pionierarbeit.
(Gabriele Rampl)